清華大學(xué)藥學(xué)院肖百龍團(tuán)隊(duì)與北京大學(xué)深圳醫(yī)院歐陽昆富團(tuán)隊(duì)合作在《神經(jīng)元》發(fā)文揭示機(jī)械力受體Piezo1的磷酸化調(diào)控及其生理學(xué)功能
2024年9月12日,清華大學(xué)藥學(xué)院肖百龍教授課題組在神經(jīng)科學(xué)領(lǐng)域權(quán)威學(xué)術(shù)期刊《神經(jīng)元》(Neuron)雜志上在線刊登了題為《Piezo1的1612位絲氨酸磷酸化調(diào)控其機(jī)械敏感性和體內(nèi)機(jī)械傳導(dǎo)功能》(Phosphorylation of Piezo1 at a single residue, serine-1612, regulates its mechanosensitivity and in vivo mechanotransduction function)的研究論文,鑒定發(fā)現(xiàn)了機(jī)械門控Piezo1離子通道中1612位絲氨酸(S1612)為響應(yīng)蛋白激酶PKA和PKC的磷酸化位點(diǎn),揭示了磷酸化對Piezo1的機(jī)械敏感性的關(guān)鍵調(diào)節(jié)作用以及對血壓和運(yùn)動耐力等生理活動的重要影響。該研究成果不僅豐富了對Piezo1調(diào)節(jié)機(jī)制的理解,也為Piezo1在血管功能調(diào)節(jié)中的潛在應(yīng)用和相關(guān)疾病的治療策略開發(fā)奠定了基礎(chǔ)。
Piezo蛋白是一類重要的機(jī)械門控陽離子通道,其能快速響應(yīng)機(jī)械力刺激,介導(dǎo)陽離子流入細(xì)胞,從而觸發(fā)細(xì)胞興奮和信號轉(zhuǎn)導(dǎo)。在哺乳動物中,Piezo蛋白家族成員Piezo1和Piezo2廣泛參與各種機(jī)械傳導(dǎo)相關(guān)活動,如觸覺感受、血壓調(diào)節(jié)等。同時,Piezo基因的遺傳突變與多種人類遺傳疾病相關(guān),如淋巴管水腫、紅細(xì)胞干癟綜合癥、觸覺缺失癥等。磷酸化調(diào)控作為常見的轉(zhuǎn)錄后修飾廣泛參與各種細(xì)胞信號通路,調(diào)節(jié)不同蛋白的活性;然而,關(guān)于Piezo蛋白如何通過磷酸化來調(diào)節(jié)其機(jī)械敏感性和生理功能的具體機(jī)制仍不清楚。
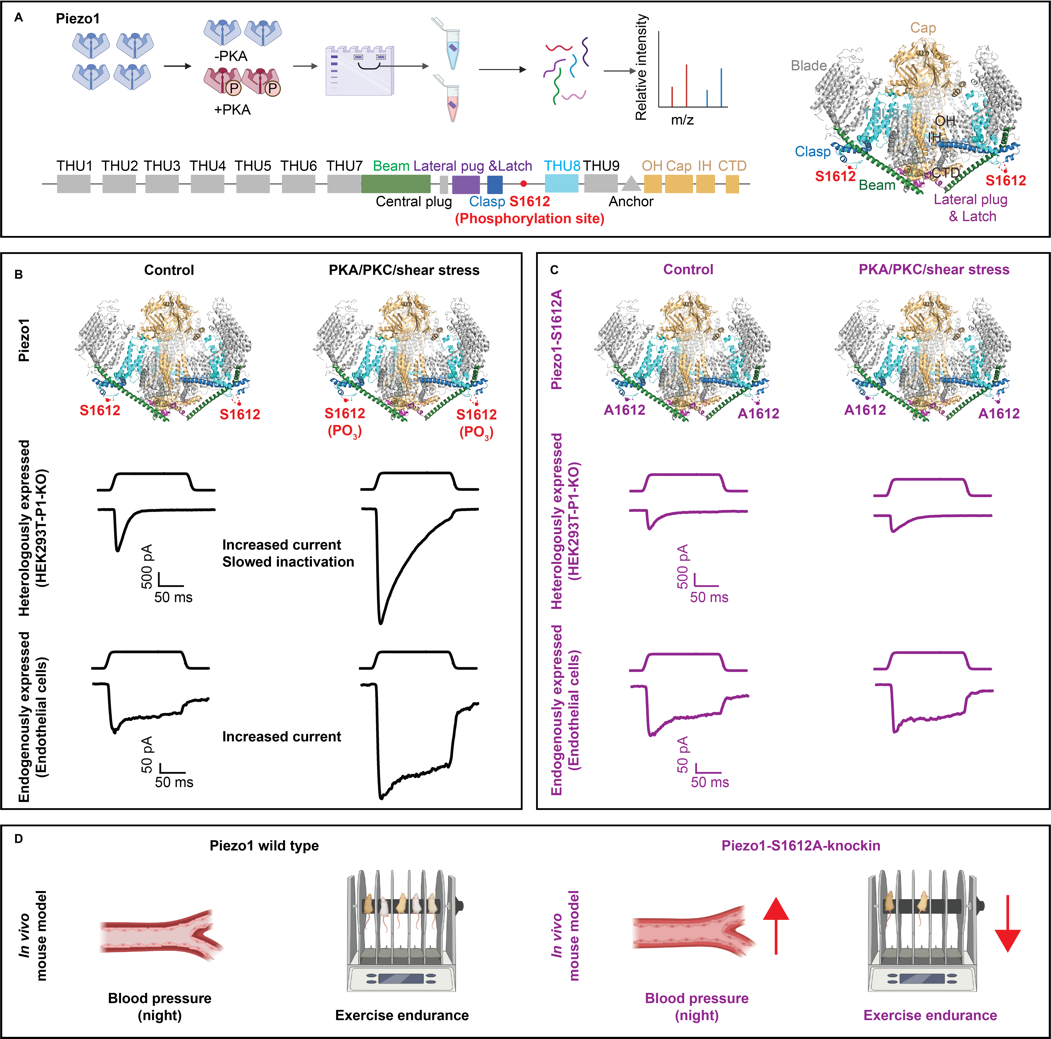
S1612磷酸化位點(diǎn)的鑒定以及S1612磷酸化對Piezo1介導(dǎo)機(jī)械激活電流的調(diào)控和生理學(xué)功能影響示意圖
在本研究中,研究人員首先探究了蛋白激酶A(protein kinase A, PKA)對Piezo1的調(diào)控。發(fā)現(xiàn)PKA激動劑8-Br-cAMP能夠顯著增強(qiáng)Piezo1通道的機(jī)械激活電流(圖B)。進(jìn)一步研究發(fā)現(xiàn), PKA通過增強(qiáng)Piezo1的機(jī)械敏感性和延長通道開放時間來提高其功能,而并未影響通道蛋白在細(xì)胞膜上的數(shù)量。
利用體外磷酸化反應(yīng)、蛋白質(zhì)質(zhì)譜分析、位點(diǎn)特異性磷酸化抗體制備、磷酸化位點(diǎn)突變并結(jié)合膜片鉗電生理分析,研究人員鑒定出S1612是PKA磷酸化Piezo1的主要位點(diǎn),其可以直接增強(qiáng)Piezo1通道的單通道開放概率來影響其機(jī)械激活電流(圖A-C)。這一磷酸化位點(diǎn)的鑒定證實(shí)了PKA對Piezo1通道活性的直接調(diào)控作用,揭示了其增強(qiáng)機(jī)械敏感性和延緩失活的分子機(jī)制。
研究人員還發(fā)現(xiàn)S1612同時也是蛋白激酶C(protein kinase C, PKC)的磷酸化位點(diǎn),能介導(dǎo)PKC對Piezo1的機(jī)械激活電流的調(diào)控。此外,機(jī)械剪切應(yīng)力及G蛋白偶聯(lián)受體激動劑(如腎上腺髓質(zhì)素、異丙腎上腺素)作為PKA和PKC信號通路的上游也可以促進(jìn)S1612位點(diǎn)的磷酸化(圖B),說明S1612位點(diǎn)的磷酸化調(diào)控方式的多樣性,也預(yù)示了其參與調(diào)控Piezo1所介導(dǎo)的生理活動的可能性。
為了進(jìn)一步研究S1612位點(diǎn)磷酸化的生理學(xué)功能,研究人員構(gòu)建了Piezo1-S1612A的突變小鼠。利用該小鼠,研究人員發(fā)現(xiàn)PKA或PKC刺激無法引發(fā)血管內(nèi)皮細(xì)胞中Peizo1磷酸化,也喪失了對Piezo1通道活性的調(diào)控(圖C)。通過與北京大學(xué)深圳醫(yī)院歐陽昆富研究員團(tuán)隊(duì)合作,對小鼠血壓進(jìn)行持續(xù)監(jiān)測,發(fā)現(xiàn)突變小鼠在夜間活動期間的收縮壓和平均血壓顯著升高。此外,行為學(xué)實(shí)驗(yàn)發(fā)現(xiàn)突變小鼠在耐力測試中表現(xiàn)出更多跌落,顯示其運(yùn)動耐力下降(圖D)。研究結(jié)果表明,阻斷Piezo1的S1612位點(diǎn)磷酸化會導(dǎo)致小鼠活躍狀態(tài)下血壓調(diào)節(jié)異常和運(yùn)動耐力的降低。
綜上,本研究鑒定出Piezo1通道中重要的磷酸化位點(diǎn),并利用生物化學(xué)分析、磷酸化抗體制備、電生理分析以及突變小鼠分析等多種技術(shù)手段,全面探究了該位點(diǎn)的磷酸化對Piezo1通道活性的調(diào)控以及在體生理活動的調(diào)節(jié),有力推進(jìn)了對Piezo1通道的精細(xì)門控調(diào)控分子機(jī)制的理解,加深了對Piezo1通道參與血壓調(diào)控和運(yùn)動耐力等生理活動的認(rèn)知,也為以Piezo通道為靶點(diǎn)的藥物研發(fā)提供了新的思路。
肖百龍教授和北京大學(xué)深圳醫(yī)院歐陽昆富研究員為本研究共同通訊作者,肖百龍課題組已畢業(yè)學(xué)生張廷鑫博士(現(xiàn)為美國得克薩斯大學(xué)西南醫(yī)學(xué)中心研究科學(xué)家),在讀博士生畢鋮和已畢業(yè)學(xué)生李祎然博士為共同第一作者。另外,歐陽昆富課題組的趙凌云和肖百龍課題組博士后崔亞雄博士也參與了部分工作。
本工作得到了國家科技部2030科技創(chuàng)新-“腦科學(xué)與類腦研究”重大項(xiàng)目(2021ZD0203301),國家自然科學(xué)基金委杰出青年科學(xué)基金以及延續(xù)資助(32425003、31825014)/重點(diǎn)項(xiàng)目(32130049)/創(chuàng)新研究群體項(xiàng)目(32021002),新基石研究員項(xiàng)目,清華大學(xué)萬科公共衛(wèi)生學(xué)院研究基金等項(xiàng)目經(jīng)費(fèi)支持。
原文鏈接:https://doi.org/10.1016/j.neuron.2024.08.009

