2025年11月29日,由清華大學尹航教授團隊牽頭,聯(lián)合海內(nèi)外學者合作完成的綜述文章《Unveiling Heterogeneity: Innovations and Challenges in Single-Vesicle Analysis for Clinical Translation》在細胞外囊泡領(lǐng)域權(quán)威期刊《Journal of Extracellular Vesicles》正式發(fā)表。該文系統(tǒng)梳理了單細胞外囊泡分析技術(shù)的最新進展與轉(zhuǎn)化挑戰(zhàn),指出微流控、超分辨成像與人工智能等方法的融合,正推動該技術(shù)向癌癥早期診斷、個性化治療及精準藥物遞送方向快速發(fā)展。
細胞外囊泡是細胞分泌的納米級載體,參與細胞間通信,其分子組成反映來源細胞的生理或病理狀態(tài)。傳統(tǒng)群體分析方法難以揭示細胞外囊泡的高度異質(zhì)性,而單細胞外囊泡分析技術(shù)能夠逐顆粒解析其表面標志物、核酸內(nèi)容物和功能特性,為疾病機制研究和生物標志物發(fā)現(xiàn)提供了全新視角。
這篇綜述重點總結(jié)和分析了以下技術(shù)方向的進展:
高通量單細胞外囊泡分離:基于微流控的開發(fā)實現(xiàn)了低樣本量(~20 μL)、高純度細胞外囊泡捕獲,有效去除非目標顆粒干擾;
多參數(shù)表型分析:納米流式與超分辨顯微等技術(shù)相結(jié)合,實現(xiàn)對單細胞外囊泡粒徑、膜秩序、蛋白組成的同步解析;
單細胞外囊泡多組學:通過DNA條形碼與液滴包裹技術(shù),實現(xiàn)單顆粒水平上百種蛋白質(zhì)的同時檢測,極大拓展了對細胞外囊泡異質(zhì)性的認知邊界;
人工智能驅(qū)動的數(shù)據(jù)分析:利用深度學習算法對海量單細胞外囊泡圖像與分子數(shù)據(jù)進行自動分類與模式識別,顯著提升分類準確性與診斷預測能力。
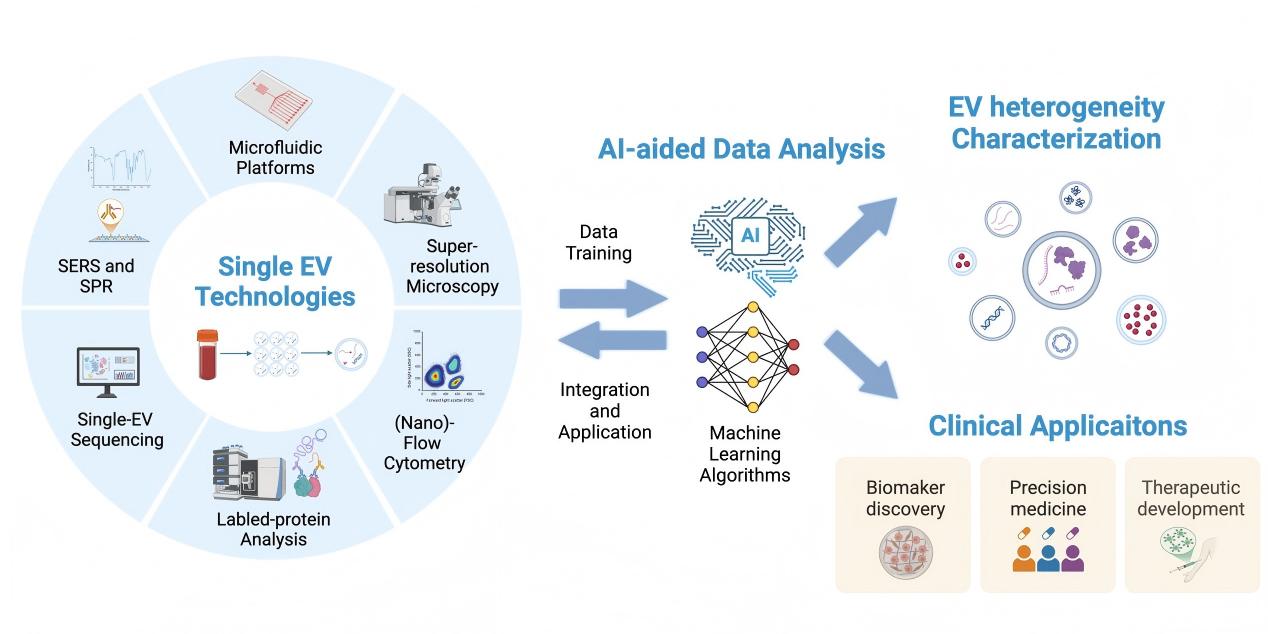
單細胞外囊泡分析在臨床轉(zhuǎn)化中展現(xiàn)出多層次價值:
1. 高靈敏度診斷:在乳腺癌、結(jié)直腸癌等模型中,成功實現(xiàn)基于表面蛋白與內(nèi)部miRNA的單細胞外囊泡檢測,準確區(qū)分早期患者與健康人群;
2. 治療監(jiān)測與個性化用藥:動態(tài)分析患者循環(huán)中的細胞外囊泡亞群變化,可實時評估藥物響應,為治療策略調(diào)整提供依據(jù);
3. 工程化細胞外囊泡作為遞送系統(tǒng):通過單顆粒水平載藥量與靶向能力的量化,推動下一代細胞外囊泡藥物的優(yōu)化與標準化。
盡管技術(shù)快速進步,該領(lǐng)域仍面臨分離標準化、檢測通量、數(shù)據(jù)整合等挑戰(zhàn)。未來,需要加強跨學科協(xié)作,建立統(tǒng)一技術(shù)規(guī)范,并推進多模態(tài)技術(shù)與AI模型的整合,以加速單細胞外囊泡分析從技術(shù)平臺向臨床工具的轉(zhuǎn)變。
本綜述的第一作者是清華大學藥學院助理研究員張瑩、博士后孟小童博士,以及澳大利亞貝克心臟與糖尿病研究所的David Greening教授。共同作者包括國內(nèi)外多位深耕細胞外囊泡領(lǐng)域研究的專家。研究工作獲得國家重點研發(fā)計劃、國家自然科學基金及北京市自然科學基金等多個科研項目的支持。
原文鏈接:https://isevjournals.onlinelibrary.wiley.com/doi/10.1002/jev2.70209?sessionid=

