2026年2月4日,清華大學(xué)藥學(xué)院尹航教授課題組在《Cell Chemical Biology》在線發(fā)表了題為“Aerobic glycolysis promotes NLRP3 inflammasome activation via NLRP3 lactylation”的研究論文。該研究發(fā)現(xiàn)了代謝物乳酸能夠直接乳酸化修飾NLRP3,從而調(diào)控NLRP3炎癥小體激活的新機(jī)制,為免疫系統(tǒng)中小分子代謝產(chǎn)物的免疫調(diào)節(jié)功能提供了新的見解。

天然免疫在抵御外來病原體感染時發(fā)揮著重要作用。細(xì)胞焦亡是細(xì)胞受到外來病原體感染時發(fā)生的一種程序性炎性死亡,對于機(jī)體抵抗病原體感染和維持穩(wěn)態(tài)十分重要。迄今為止,已經(jīng)有多種模式識別受體被證明能夠響應(yīng)多種刺激形成炎癥小體介導(dǎo)細(xì)胞焦亡,其中NLRP3是NLR家族蛋白中重要的組成成員之一。NLRP3的激活需要兩個步驟:啟動步驟和激活步驟。首先,NLRP3可以被核轉(zhuǎn)錄因子(Nuclear factor kappa B,NF-κB)或其他轉(zhuǎn)錄因子激活后誘導(dǎo)表達(dá)。第二步是激活階段,NLRP3可以被多種刺激物所激活,包括細(xì)菌毒素如尼日利亞菌素、細(xì)胞外ATP、MSU、膽固醇結(jié)晶和淀粉樣蛋白等顆粒物。一旦激活后,NLRP3招募下游蛋白組裝成炎癥小體復(fù)合體,引發(fā)細(xì)胞焦亡和下游炎癥反應(yīng)。但是過度的細(xì)胞焦亡也會出現(xiàn)炎癥表型,包括臨床上敗血癥后期出現(xiàn)的炎癥因子風(fēng)暴等,因此細(xì)胞焦亡的調(diào)控也是重要的科學(xué)問題。近年來,越來越多的研究發(fā)現(xiàn)免疫細(xì)胞發(fā)揮功能的同時伴隨著代謝改變,代謝小分子也被報道參與到免疫調(diào)節(jié)的過程中,免疫與代謝的密切聯(lián)系越來越是值得關(guān)注的問題。
研究團(tuán)隊通過研究巨噬細(xì)胞焦亡的代謝特征定位到差異代謝物乳酸,系統(tǒng)性研究了乳酸對巨噬細(xì)胞焦亡的調(diào)控和分子作用機(jī)制。作者分別通過化學(xué)干預(yù)和基因敲降的方式對細(xì)胞內(nèi)乳酸生成進(jìn)行調(diào)控,發(fā)現(xiàn)乳酸調(diào)控NLRP3炎癥小體激活介導(dǎo)的細(xì)胞焦亡而不影響AIM2炎癥小體的激活。在機(jī)制研究上,作者定位到乳酸會促進(jìn)NLRP3招募下游接頭蛋白ASC和激活,通過免疫印跡分析發(fā)現(xiàn)NLRP3蛋白存在乳酸化修飾,并且NLRP3與乳酰轉(zhuǎn)移酶AARS2存在相互作用。作者進(jìn)一步通過質(zhì)譜鑒定到了NLRP3的乳酸化位點并對這些位點進(jìn)行突變驗證以及在巨噬細(xì)胞中進(jìn)行了功能學(xué)驗證,發(fā)現(xiàn)在Nlrp3-/-的iBMDMs細(xì)胞中穩(wěn)轉(zhuǎn)了K24R和K565R雙突變NLRP3后能顯著抑制NLRP3激活介導(dǎo)的細(xì)胞焦亡,并且能明顯減弱NLRP3的乳酸化程度。隨后在小鼠多菌群感染的疾病模型中,研究團(tuán)隊也證明了乳酸對疾病的影響。
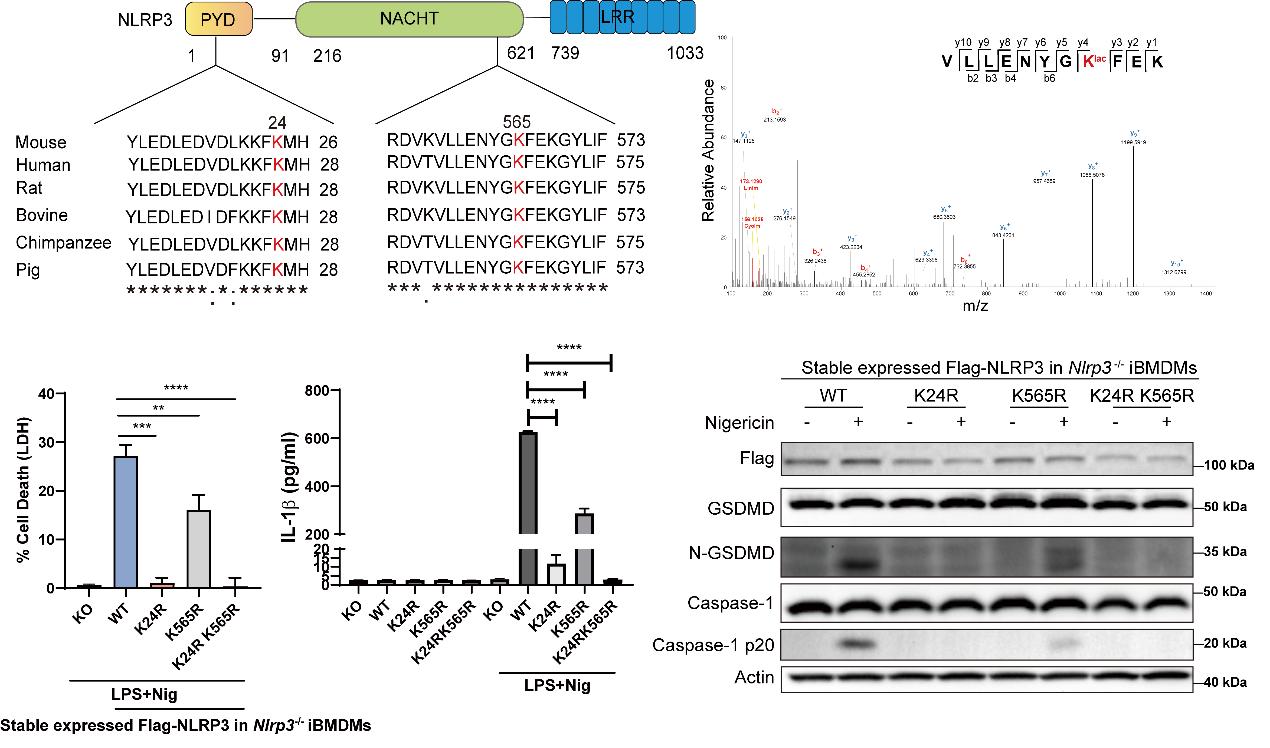
綜上,本研究發(fā)現(xiàn)糖酵解通路代謝產(chǎn)物乳酸的能夠通過乳酸化修飾NLRP3,調(diào)控NLRP3炎癥小體的激活以及下游的炎癥反應(yīng),為免疫系統(tǒng)中小分子代謝產(chǎn)物的免疫調(diào)節(jié)功能提供了新的見解,為焦亡相關(guān)疾病的藥物開發(fā)提供新思路和新靶標(biāo)。
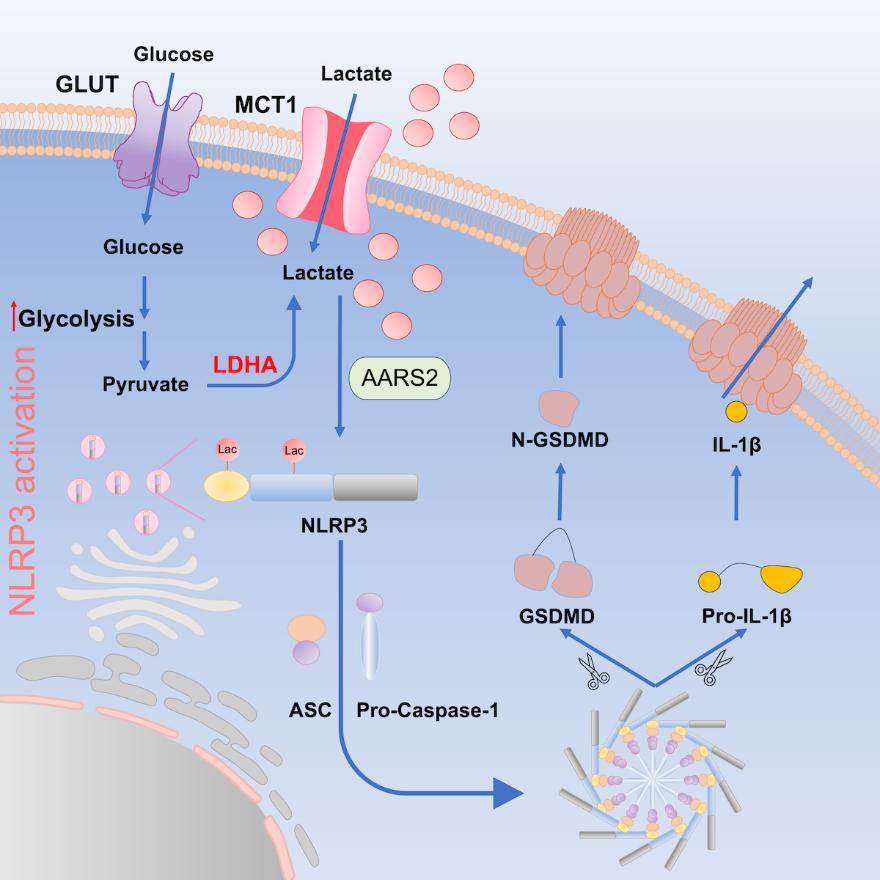
清華大學(xué)藥學(xué)院尹航教授為本文通訊作者,清華大學(xué)藥學(xué)院已畢業(yè)博士劉薇為該論文第一作者。清華大學(xué)藥學(xué)院在讀博士生張?zhí)煲缓颓迦A大學(xué)藥學(xué)院胡澤平課題組王博弘博士為本項目的順利開展提供了重要的技術(shù)支持。本研究獲得了國家自然科學(xué)基金、國家科技重大專項等項目的資助。
原文鏈接:https://www.sciencedirect.com/science/article/abs/pii/S2451945626000231?dgcid=author&sessionid=

